化学の受験勉強を始めたいと思ったけれど、何からしたら良いのか分からない。
学校の定期試験は大丈夫だけれど、模試で点数が全然とれない。
この悩みを解決するため、講師歴15年の著者が勉強法を紹介します。
なお、本ページの受験スケジュールに関しては東大・京大などの超難関国公立大学、医学部受験は本ページの対象外です。
地方国公立・MARCH・関関同立の受験生が該当します。
1年間では到底間に合いません。別ページにて解説する予定です。(2023/02/08地点)
著者は現在も予備校や医学部専門の完全個別指導で、化学を教えています。
受験化学は、膨大な量の勉強する事柄があるため、
ただ闇雲に勉強しても受験までに勉強が間に合わない可能性が・・・。
この記事を読むことで、少しでも効率よく勉強できたらと願います。
・ 初学者は教科書が基本。それがツラいなら講義系参考書を中心に勉強します。
無機化学は教科書の学習の前に、予備知識を入れておきましょう。
・ 教科書を 1 章終わらせる毎に、必ず問題集で問題演習をします。
・ 化学は量が多いです。夏からの勉強は遅すぎます!どんなに遅くても 高2の 3 月から始めましょう。
・ 著者が 2022 年地点で一番オススメなのは化学の良問問題集です。
先に読みたい人は >>コチラから。
「化学」の4領域と、「化学」という教科の特性

化学の4領域とそれらの関係
化学はとにかく学習内容が多いです。化学の単元を大きく4つに分けると次のようになります。
- 理論化学(暗記2割)
- 無機化学(暗記8割)
- 有機化学(暗記3割)
- 高分子化合物(暗記6割)
暗記の割合は著者の感覚。発展的な理論(大学初年度程度の内容)が理解できればもう少し暗記の量は減りますが、
東大・京大・医学部単科の志望で化学を得点源にしようとする人以外は暗記に頼る方が良いでしょう。
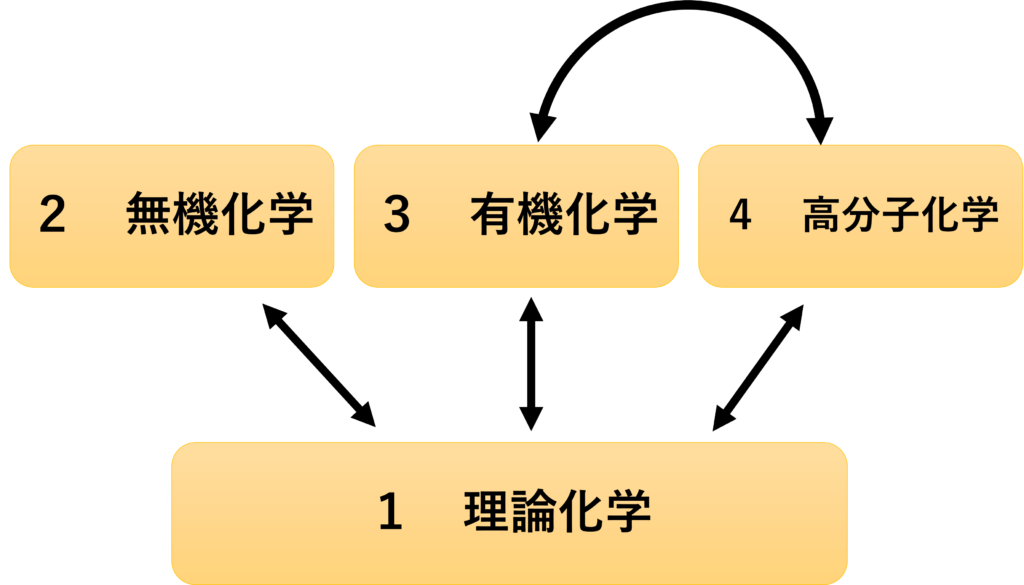
1の理論化学の知識は他の2、3、4でも一部使います。
また4の高分子化合物は、そのほとんどが有機化合物を扱うので3の知識を一部使います。
しかしそれぞれが独立している単元も多いので
最悪いずれか1つの領域を捨てて、他の3つの領域で入試の点を取りに行くという戦略もあります。
このとき理論化学を捨てることはできません。配点の半分以上が理論化学ということは珍しくないからです。
領域を捨てるかどうかに関わらず、化学の勉強は理論化学を優先するべきです。
化学の各領域(理論・無機・有機・高分子)の勉強法と注意点
予備校・塾に通っている人は、授業を担当する講師が勉強法(予習・復習の方法)を説明してくれるので忠実に守るべきです。
講師の授業はその勉強法をしている人にとって最大限効率が良くなるように組み立てていることが多いです。
生徒側が別の勉強法を使ってしまうと、かえって非効率に。
以下の記事は主に独学をしている、または講師から特に勉強法を言われていない人向けです。
理論化学

初学者の場合は学校教科書をしっかり読み込んで理解していきます。
侮ってはいけません。
著者も数年ごとに読破していますが、教科書は丁寧にしっかり書かれています。
年々、図が豊富になってきており、頭に入りやすい工夫がされている印象。
何も知識が無い人がイチから勉強する教材として、
学校教科書は最適です。
しかし、文章を読むのがツライ人も居ます。
そのような場合は、図解が多い講義系参考書を使うと良いです。
理論化学の単元を読み込むときには次の点に注意してください。
- 新しい概念がでてきたら、既に持っている知識にとらわれずに素直に受け入れる。
特に定義が示されていたら、1字1句正確に覚えて人に説明できるようにする。 -
具体例
A とは B である。といった文章は定義を述べていることが多いです。
例) 「中和熱とは酸と塩基が中和して 1$ \mathrm{\ mol} $ の水が生成するときに発生する熱量のことである。」この文章を読んだときに、
あ〜、中和熱っていうのは中和するときの熱か。そのままだな。
と流しているようでは、問題を解けるようにはなりません。
「1 $ \mathrm{\ mol} $ の水が生成するとき」という文も含めて覚えないと次の問題でつまずきます。
例題$0.50 \mathrm{\ mol } $ の塩化水素と $0.30 \mathrm{\ mol} $ の水酸化ナトリウムが反応するときに生成する熱はいくらか。
ただし中和熱を $56.5 \mathrm{\ kJ/mol } $ とする。単位だけを見たときに、$56.5 \mathrm{\ kJ/mol } $ に対して何の $ \mathrm{\ mol} $ を掛ければいいか分からなくなる人が多いです。
中和熱の定義は水 1 $ \mathrm{\ mol} $ あたりの熱量であるから、水が $0.30$ mol 出てくることに注意して
$$56.5 \mathrm{\ kJ / mol} \times 0.30 \mathrm{\ mol} = 16.95 \mathrm{\ kJ}$$
定義は自分で勝手に省略せず、全て記憶しましょう。 - 新しい単位や公式が出てきたら、式中の単位と、何を表す単位なのかを意識する。
-
具体例(単位)
(1)モル濃度が $1.0 \mathrm{\ mol / L }$ の $\ce{NaOH}$ 水溶液が $100 \mathrm{\ mL} $ ある。この水溶液に含まれる $\ce{NaOH}$ は何$\mathrm{\ mol}$か。有効数字2桁で求めよ。
モル濃度は $ \dfrac{\text{溶質の物質量} \mathrm{\ mol }}{\text{溶液の体積} \mathrm{\ L} }$ で表されるから、モル濃度に溶液の体積をかけると、溶質の物質量 $\mathrm{\ mol }$ が計算できる。
$$1.0 \mathrm{\ mol / L} \times \dfrac{100}{1000} \mathrm{\ L} = 0.10 \mathrm{\ mol} $$
(2)$0.40 \mathrm{\ g}$ の $\ce{NaOH}$ を $49.6 \mathrm{\ g} $ の水に完全に溶かして水溶液を作った。この水溶液の質量モル濃度は何 $ \mathrm{\ mol / kg}$ か。有効数字3桁で求めよ。
質量モル濃度は $ \dfrac{\text{溶質の物質量} \mathrm{\ mol } }{\text{溶媒の質量} \mathrm{\ kg} } $ で表されるから、溶質の物質量を溶媒の質量で割ると、質量モル濃度が計算できる。
$$ \dfrac{0.40 \mathrm{\ g}}{40 \mathrm{\ g/mol}} \div \dfrac{49.6}{1000} \mathrm{\ kg} = 0.2016 \cdots $$
$$0.202 \mathrm{\ mol / kg} $$
濃度の分母がいつの時でも溶液(全体)と思っていると痛い目に遭います。
質量モル濃度の分母は溶媒(水)なので、 $0.40 \mathrm{\ g} + 49.6 \mathrm{\ g} = 50 \mathrm{\ g} $ として溶液の数値で計算してはいけません。(この値で計算すると $0.200 \mathrm{\ mol / kg} $ となり誤り。)
公式は、何に関する単位であるのかも合わせて覚える必要がある!。
1章分読めたら、学校配布の基礎的な問題集(セミナー化学やリードα)を用いて
今読んだ章に該当する問題を解いていきます。
教科書に書いてあったことを思い出しながら、解ける問題を解きましょう。
もちろん分からない問題があってもOKです。
大問を1つ解くごとに必ず答え合わせをして、答えが合っているかどうかに関係なく解説を読み込みましょう。
計算問題のときは、自分の解いた方法と解説の方法を比べて
より確実に解ける方法を今後使えるようにしたいです。
どちらも確実に解ける方法なのであればより速く解ける方を採用しましょう。
間違っている問題に関しては、次同じ問題が来たときに答えられるように。
問題番号にチェック✅をつけたり、間違いノートを作るなどして
あとで復習しやすい状況にしておくと良いです。
解説を読んでも分からない場合は、講師や友人に質問してみるのも良いでしょう。
また、当ブログでは一部の単元ですが解説記事を投稿しています。
パターン別に問題の解法を載せているので下の記事も参考にしてみてください。
■ ヘンリーの法則の公式といろいろな問題の解き方
■ リチウムイオン電池の問題
計算問題について


化学の入試の計算においては、ほとんどが文字ではなく数値で与えられます。
ゆえに単純な「足し、引き、掛け、割り」の四則計算を
正確にかつ迅速に解く能力が必要です。
ピストン付き容器の中に、$\pu{6.0E4 Pa}$ で $27$℃ の酸素が $\pu{1.5 mol}$ ある。このときの体積は何 $\pu{L}$ か。気体定数は $R = \pu{8.3E3 Pa*L/K*mol}$ とする。
気体の状態方程式 $PV = nRT$ を変形した $V = \dfrac{nRT}{P}$ に各数値を代入すると、
$$V = \dfrac{1.5 \times 8.3 \times 10^3 \times (27 + 273)}{6.0 \times 10^4}$$
10の●乗とそれ以外の部分を分けて
$$V = \dfrac{1.5 \times 8.3 \times 3}{6.0} \times 10 $$
$1.5$ と $6.0$ を約分して $8.3$ と $3$ を掛けて
$$V = \dfrac{0.5 \times 24.9}{2} \times 10 \hspace{5mm} $$
$$V = 62.25$$
有効数字2桁として、(答)$62 \ \mathrm{L}$
これ以上に複雑な計算もでてくる(密度や濃度)ので、
上記に示したように約分や10の指数を分ける方法は習得しておきたいです。
計算能力はすぐに身につくものでは無いため、
普段の演習でも電卓を使わずに手計算で練習する必要があります。
とはいえ初めて勉強する単元で難しく感じ、理解に時間がかかるのであれば、電卓を使ってOK!
その単元の理解を最優先するべきです。
メリハリをつけて電卓と上手く付き合いましょう。
なお当ブログでは計算のケアレスミスに関する記事を扱っています。
有効数字について
基礎なしの化学が入試で必要なのであれば、
全ての計算問題において有効数字を守った答え方をしましょう。
著者は大学別の記述模試の採点をしていますが、
答案に有効数字違反があった場合、容赦なく減点しています。(基準に定められている。)
入試でどうなるかは分かりませんが、
減点される可能性を下げる努力はするべきです。
ざっくりとしたルールは以下の通り。
数字を左から見ていって初めて 0 でない数字が現れたら、そこから数えた桁数が有効数字の桁数である。
左の方の 0 は位取りの 0 であり、有効数字に含めない。
・ $3.14$ の有効数字は 3 桁である。
・ $0.025$ の有効数字は 2 桁である。(左 2 つの 0 は有効数字に含めない。)
0 でない数字の右側に 0 が現れても、その 0 は有効数字の桁数に含める。
・ $1.00$ の有効数字は 3 桁である。 ( 1 の右側の 0 は全て有効数字に含める。)
・ $0.0250$ の有効数字は 3 桁である。
( 2 の左側の 0 は有効数字に含めないが、5 の右側の 0 は有効数字に含める。)
無機化学


初学者は教科書を読んでいきますが、その前にして欲しいことがあります。
それは、無機化学に特化した参考書・または(当ブログのような)WEB サイトを使って
理論化学と無機化学を結びつけ単元を予備知識として学習するということです。
前知識が無い状態で教科書を読み進めていくと、「全てを覚えないといけないのか」となって挫折しやすいです。
無機化学の特徴として暗記すべき事柄が多いということが原因にあります。
ただし丸覚えしないといけない事柄と、そうでない事柄とが存在します。
丸覚えするべき事柄
- 気体や水溶液の色
- 水に溶けにくい沈殿ペアの組み合わせ
(水中では$\ce{ NaCl }$ は溶けるが、$\ce{ AgCl }$ は難溶である、など。) - 錯イオンの作り方
(錯イオンが絡む反応式を作るものはある程度の手順がある。)
丸覚えすべきではない事柄
- 化学反応式・イオン反応式を作る
(ほんの一部暗記のものもある。) - 実験操作
- その他、高校の理論化学で説明できる事象
注意してほしいのは、「丸覚えすべきではない」ということは「暗記不要」という意味ではありません。
何か1つの『知識・解法』を理解(暗記)して、他にその『知識・解法』を適用できることがあるので、
個別に丸暗記をしなくても良い、ということです。
具体例は以下をクリック。
具体例(弱酸の遊離反応)
理論化学の知識を利用すると次の弱酸遊離反応が進むことがわかる。(その過程は省略)
弱酸(弱塩基)の塩 + 強酸 → 弱酸 + 強酸の塩
$\ce{ CaCO3 + 2HCl -> H2O + CO2 ^ + CaCl2}$
$\ce{ Na2SO3 + H2SO4 -> H2O + SO2 ^ + Na2SO4 }$
$\ce{ CH3COONa + HCl -> CH3COOH + NaCl}$
$\small{\ce{ 2NH4Cl + Ca(OH)2 -> 2NH3 ^ + 2H2O + CaCl2}}$
この4つの化学反応式はいずれも弱酸遊離反応で作ることができます。
1つの事を覚えたら4つの問題が解けたことになります。
この暗記の核となる『知識・解法』は教科書にまとまって載っているわけではありません。
そこで市販の参考書やインターネットサイトでこの知識を学習する必要が出てきます。
参考書は「Do シリーズ 福間の無機化学」、インターネットサイトは受験の月がオススメです。
無機化学の暗記の核となる『知識・解法』がある程度習得できてから、教科書や講義系参考書を読んでいきましょう。
化学反応式や実験操作が登場したら、
覚えた『知識・解法』の中の何を使っているのかを考えましょう。
教科書を 1 章分読めたら、基礎的な問題集(セミナー化学やリード α)で問題演習に入っていきます。
演習を積んでいけば似たような問題によく当たるようになります。
そうすると、例えば化学反応式を答える問題に関して
イチから作ることもできるけれど、自然と結果を覚えてしまっていてスラスラ書ける!!
という最高の状態になります。ぜひこの状況を目指してほしいと思います。
無機化学に関して以下の記事を公開していますので、参考にしてください。
■【高校化学】錯イオンとは何か〜イオン式の作り方〜
■ 錯イオン・錯塩に関するイオン反応式、化学反応式の作り方
有機化学

まず教科書や講義系参考書を読みます。
はじめに覚えるべき内容を挙げます。
- 官能基の式と名称。
- 異性体。異性体の書き出しがある程度できるようになるとOK
- アルカン $\ce{C_{n}H_{2n+2}}$ の名前を $n = 6$ まで。
- 有機化合物の名前の付け方のルール。
- 有機化合物の慣用名。
無機化学で手に入れた「知識・解法」は有機化学でもある程度は使えます。
しかし有機化学の反応に関しては、
本質が『電子 $\ce{e-}$ の振る舞い』にあります。
どういった状況のときに、電子はどう動くのか?
というのを学習するする必要がありますが
初学者には難易度が高いです。
京大・東大・単科医学部受験者でなければ、
反応はある程度簡略化して暗記する方が良いです。
また、有機化学は全体として反応が繋がっています。
『反応経路図』というのが、資料集や教科書にあるので
何も見ずに書けるようになることが、有機化学の勉強の目標の1つです。
問題集で章ごとの問題演習をするときに構造決定の問題がでてきます。
基本的なものは解いても良いですが、
発展問題に出てくるような入試の過去問ほどの長文の問題は一旦飛ばしましょう。
化学を全て一周してから再び有機化学に取り組むときに
構造決定を解くコツを頭に入れてから取り組む方が効率が高いです。
習いたてのときに取り組むと、時間がかかりすぎることが多いので
1週目に構造決定をたくさん演習するのはおすすめしません。
有機化学に関して以下の記事を公開していますので、参考にしてください。
■ 不飽和度について
高分子化合物


やはり教科書か講義系参考書を読んでいきます。
構成としては
「単量体の性質 → 重合体の作り方とその性質」
(糖の場合は、単糖 → 二糖 → 多糖)
という流れになっています。
重合体が「何の単量体からできているのか」を理屈抜きにしっかり覚える必要があります。
知識を身につけたら計算問題にも取り組みましょう。
具体例(単量体と重合体 / 単糖と二糖)
糖における例 α – グルコース + β – フルクトース → スクロース
天然高分子における例 ヌクレオチドどうし → 核酸(ポリヌクレオチド)
合成高分子における例 ヘキサメチレンジアミン + アジピン酸 → ナイロン66
これらは「なぜナイロン 6 6 を作るのに他のカルボン酸ではなくアジピン酸を使うのだろう?」とか考えてはいけない。(本当に考えたいのであれば、受験が終わってから。)
理屈抜きに「何と何で、何ができるか」を覚えていこう。
受験化学の勉強の一般的な年間スケジュール


※本ページの受験スケジュールに関しては東大・京大などの超難関国公立大学、医学部受験は本ページの対象外です。
別ページにて解説する予定です。
受験勉強の計画を寝る前に、まずは明確に志望校を決定しましょう。
人生を左右することなので慎重に選ぶことは大事なのですが、
目標が有るのと無いのとでは勉強方針や日常生活の送り方が変わってきます。
志望校が決めきれないという人は、
少しでも成功に近づけるために短期目標でも良いので立てるようにしましょう。
(例)
・ 6 月のマーク模試で偏差値 50 を切らないようにする。
・次の模試で関関同立の判定を D 以上にする。
目標を立てると良いという記事を公開していますので、
勉強法が理解できたらで良いので読んでみてください。
受験年度の 3 月で、ほとんど知識がない・化学に自信が無い人向け
理論化学と無機化学を学校教科書・基礎問題集で進めます。(発展問題は不要)
単元によっては少々取りこぼしがあっても良いです。
7 月末までに理論を終わらせる目標で勉強しましょう。
有機化学を学校教科書・基礎問題集で進めます。(発展問題は不要)
周りは過去問を始めたりするかもしれないですが、焦る必要はありません。
有機・高分子がまだ途中であれば学校の進度に合わせて進めます。
終わっていれば教科書・基礎問題集で最後まで進めましょう。
はじめに、志望校の過去問を 1 年分演習しましょう。
必ず時間を測ってやってください。正答率が低いとか高いとかで一喜一憂してはいけません。
問題の難易度はどれくらいか。どのような出題形式か。(マーク・記述)
時間は余裕があるのか、全然足りないのか。
この辺りを分析しましょう。
その後、基礎問題集の 2 週目を進めます。
1週目でチェック ✔ をつけたところや、苦手な単元のみ解きましょう。
それが終われば問題集のレベルを上げます。
基礎問題精講か、良問問題集を使うと良いです。
各々の受ける入試(共通テストも含む)の対策問題・過去問演習をします。
間違い直しのときに「ここの単元が弱い」などの課題が見つかるので
適宜、使っている問題集で該当単元を復習しましょう。
受験年度の 3 月で教科書内容が全単元終了していて、ある程度自信がある人向け
全単元を、基礎問題集(セミナー化学など)で進めます。
明らかに分かる問題(単なる mol の変換問題など)は飛ばします。
ただし単元を丸ごと飛ばすのは良くありません。
知識の穴を埋める作業だと思って問題を確認しましょう。
少しでも解き方があやふやだろうという問題は飛ばさずに演習しましょう。
標準レベルの問題集を使って、全単元進めます。
この地点で発展レベル(重要問題集のB問題や良問問題集のレベルアップ問題など)は演習しなくて良いです。
場合によっては 10 月末までもつれ込んでもOK。
なお重要問題集などに見られる有機化学の構造決定問題ゾーンは、「必」マークのみやりましょう。
全てやろうとすると心の折れる人が多いです。
標準レベルの問題集の発展問題以外・重要問題集の A 問題が終われば、難関大学志望者(目安:全統模試偏差値57.5程度以上)は過去問を 3 年分やって出題内容を分析したのち、発展問題(重要問題集のB問題や良問問題集のレベルアップ問題)に取り組みましょう。毎年出題されるような単元があれば、その単元を重点的に演習します。
それら以外の大学の志望者は、志望大学の2次試験の過去問に取り組みます。
本命は3年分・併願校は1年分を目安に解きます。
必ず時間を測ってやってください。正答率が低いとか高いなどで一喜一憂してはいけません。
問題の難易度はどれくらいか。どのような出題形式か。(マーク・記述)
時間は余裕があるのか、全然足りないのか。
この辺りを分析しましょう。
苦手な単元などがさらに浮き彫りになってくるので、
適宜手持ちの問題集で復習しましょう。
共通テスト対策問題集などで演習しましょう。
共通テストが不必要な人、または共通テストが終われば、
2次試験・個別試験に向けて過去問演習や知識の穴を埋める勉強を進めていきましょう。
過去問演習の効果的な方法 | 解いて丸付けして一喜一憂は厳禁


過去問演習は大きく分けて2つの手段があります。
- 市販の本を購入する。教学社のいわゆる「赤本」が代表的。共通テストや旧帝大は駿台文庫の「青本」もある。
- Web サイトを利用する。東進が運営している、「大学入試問題過去問データベース」が代表的。
大体の大学の入試問題の PDF と解答が無料で利用できる。年度によっては解説も確認できる。
どちらの手段でやるにしても、過去問演習の方法は以下の通りですればOKです。
制限時間がきたら分かるように、タイマーをかけてやりましょう。時間が来たらすぐにペンを置いてどこまでできたかチェックをすること。
あと何分あれば解けたのかが分かる。各大問の最後の問題は自分にとって解けるものであったのかも確認できる。
制限時間内で何%の正答率だったのかを記録する。全科目合わせて、その年度の合格最低点を上回っているかを確認。
10%以上足りていないのならばまだ実力不足。過去問演習の前に問題集に戻って該当単元の問題演習をして知識の穴を埋めること。
解説を読んで自分の解き方と比較する。それが自分の知識に無いもので、その解き方のほうが速く解けるものであれば、自分が使えるようにする。
化学に関して、過去問演習の解説が分からなかったり、そもそも解説が手元にない場合は当ブログで(ほんの少しではあるが)記事を公開しています。今後も記事を増やしていく予定です。
2022 年 大阪公立大学
2019 年 大阪医科大学
2019 年 関西医科大学
2020 年 大阪大学
2012 年 大阪大学
2019 年 立命館大学
化学のおすすめ参考書


著者が今まで完全個別指導などで使用してきた問題集から、オススメの問題集をピックアップします。
予備校・塾に通っている人
基本的には、配布されるテキスト・冊子・プリントを信じて勉強していきましょう。
授業のレベルが全然合わない(簡単すぎる or 難しすぎる)のであれば、
以下のレベルに合わせて追加購入して学習しましょう。
基礎レベル | 宇宙一わかりやすい高校化学(Gakken)
初学者用の講義系参考書。
絵や図がたくさん使われていて、文章を読むのが苦手な人にとって良い参考書です。
「宇宙一分かりやすい」という言葉のせいで怪しく感じますが、
講義内容は真っ当です。安心してください。
理論・無機・有機と分冊になっていて、それぞれの単元で抑えるべき基礎的な内容は網羅されています。
講義系ということで圧倒的に問題数が少ないので、セミナー化学などの基礎レベルの問題集で問題を解きましょう。
標準~発展レベル|旺文社Doシリーズ
教科書の文章を読むのが苦ではないけれど、イマイチ頭に入ってこない・要点がつかめないというのであればコチラ。
予備校講師が書いた本で
授業の内容や板書をそのままセリフ・図にしたものだから頭に入りやすいです。
2次試験で化学を使う人向け | 無機化学の勉強に入る前の必須教材
無機化学は全てが暗記というわけではありません。
理論化学の知識を借りると暗記しなくても済む事項があります。
その知識の使い方をこのテキストでは教えてくれます。
第1章の「無機化学を学ぶにあたって」と第2章の「化学反応式を作ろう」は必ず習得しましょう。
(ちなみに化学を入試で使うのが共通テストのみであるとか、
化学がかなり苦手というのであれば、無機化学の全て丸暗記に頼るのもありです。)
これを終えれば続けて第3章に進むのも良いし、教科書に進んでも良いです。
無機化学の勉強の暗記に対する負担が軽くなります。
高校化学の辞書|理系大学受験 化学の新研究 (三省堂)
初めから読破する目的で使ってはいけません。
教科書や問題の解説で更に突っ込んだ知識が知りたいときに辞書として使いましょう。
息抜きで「SCIENCE BOX」のコラム記事を読むことは
2 次試験の題材になりうるものなのでOKです。
高校化学の最上級参考書|新理系の化学(上)(下) (駿台文庫)
化学を超得意科目にしたい、もしくは化学を教える大学生や講師の人にとって良い1冊。
各単元を本当にイチから解説しています。
「イチから」というのは大学内容も入っているため、初学者には敷居が高いです。
忠告ですが、「自分は化学がデキるから難しいのをやろう」という中途半端な学力の人がやると間違いなく無駄に終わります。
「受験化学」を1年間で取り組もうとしている大多数の人にはおすすめしません。
しかし真正面からサイエンスという「学問」をしようとする人にとっては凄くオススメ。
大学内容に踏み込むときもイラストや例えが使われるので,高校生でも理解は可能です。
万が一この参考書を使うのであれば、少なくとも 2 年間は時間が欲しいです。
理解が進めば少なくとも化学に対して、根本的・統一的な理解が得られるでしょう。
化学のおすすめ問題集
基礎レベル | セミナー化学(第一学習社) or リードLight ノート(数研出版)
セミナー化学は、化学を全く勉強したことがない人でも
教科書と併用すれば十分に使うことができる問題集です。
各章のはじめのページに、単元のざっくりとした説明がありますが、
さらっとまとめているだけです。
教科書で1章分読んで内容をある程度理解してから
その章の問題に入りましょう。
リード Light ノートも日常の勉強から使える問題集。
特徴は、各章のはじめが穴埋めのページになっていて
その章で学習する内容や用語の整理ができるところです。
初めて問題に取り組むときは、リードCまでの問題を確実に答えられるようにしていけば大丈夫です。
標準レベル | 化学(化学基礎・化学)基礎問題精講(旺文社)
「基礎」と名前が付けられていますが、レベルは MARCH や産近甲龍あたりを目指す人のための問題集と考えて良いです。
入試問題を解くための「基礎」問題という位置づけ。
したがって現役生が日常学習として使うにはハードルが高いです。
高卒生(浪人生)で前の年に化学がそこそこ出来ていたのであれば、
以下2つの問題集の前段階として使うのはOK。
問題を解く道筋はきちんと書かれているので
答えそのものを覚えるのではなく、答えに至る道筋をしっかり覚えていきましょう。
標準 〜 発展レベル | 化学の良問問題集(旺文社)
河合模試で偏差値 55 駿台模試で偏差値 50 ほど出ているなら使ってよい問題集。
標準的な問題から難関大まで網羅しています。
まずは確認問題と必須問題をしっかり演習したうえで、入試までにレベルアップ問題に取り組みたいです。
解説も非常に丁寧に書かれているので、独学しやすいです。
著者が2022年現在最もオススメする1冊です。
標準 ~ 発展レベル | 化学(化学基礎・化学)標準問題精講(旺文社)
河合模試で偏差値 55 駿台模試で偏差値 50 ほど出ているならこのレベルの問題集に取り組むと良いでしょう。
難関大で出題される問題のパターン問題は、全ての単元で網羅されています。
次に挙げる重要問題集と比較すると解説はかなり丁寧です。(できる人にとっては冗長と感じるかもしれないが。)
また、図も綺麗で見やすいです。重要問題集には図が少ないかあっても小さいので、これもメリットの1つに挙げられます。
標準 〜 発展レベル | 実戦化学重要問題集 化学基礎・化学(数研出版)
いわゆる「老舗」。多くの受験生が利用しているといっても過言ではない問題集です。
もし学校指定でこの問題集を購入していて学校でいくらか演習済みであり、
河合模試で偏差値 55 駿台模試で偏差値 50 ほど出ているなら
この問題集で入試まで進めても良いです。
入試標準的な問題から難関大のパターン問題がほぼ網羅されているので
入試直前まで利用する価値はあります。
デメリットとして、問題数があまりにも多く消化不良を起こしやすいということと、
解説がやや難しく感じる問題が散見されるという点が挙げられます。
問題集の進度管理と質問を受けてくれる人が居る環境であれば、
このデメリットはほぼ解消されます。
手元にこの問題集がなく、今から手に入れようと考えているのであれば、
上記の「標準問題精講」か「良問問題集」をおすすめします。
化学のおすすめ動画


無料動画
特定の単元がわからないときは、YouTube などの動画を利用すると良いです。
- 長くても 20 分以内で見られるので、スキマ時間で確認できる。
- テキストを目で追うだけではなく、音声からも情報が入ってきて理解しやすい。
- 倍速機能を使って気になるところのみ通常再生することで時間短縮。
(シークバーで飛ばすのはオススメしない。大事な前提条件を見逃してしまう。)
オススメの YouTube 動画 (無料)を紹介しているので参考にしてください。
有料動画
駿台予備校などの大手予備校で教えていた(教えている)講師が講義をしている動画サイトも存在します。
有名なものには、スタディサプリや学研プライムゼミ、オンライン家庭教師メガスタ などがあります。
これらは有料で、月額もしくは年額を支払って受講します。
講師は大手予備校・塾での出講を経験したベテランであることが多く、
無料動画を上回るハイクオリティな講義を受けることができます。
当ブログではスタディサプリの解説記事もあるので、気になる方は下の記事もどうぞ。


デメリットもあります。
実際の予備校のように強制力がないので、
自分に甘い人はいくらでも休憩できてしまいます。
「みんチャレ」のようなアプリを使えば
チームで勉強報告をし合うようなシステムがあるので
このデメリットを克服しやすいです。
実際の予備校と比べれば料金は安いので、
予備校選びの候補として考えても良いでしょう。















