第1問
(1) A(ウ) B(イ) C(ウ)
※ C : $\ce{SiO2 + 6HF -> H2SiF6 + 2H2O}$ は酸との反応とみなした。
(2) A(ア) B(オ) C(ア)
(3) A(イ) B(ウ) C(ア)
C : $r$ を原子半径、$l$ を単位格子の一辺とおくと、$\dfrac{\sqrt{3} l}{4}=2r$
$r = \dfrac{1.73\times5.4\times10^{-8}}{8} = 1.167\times10^{-8}$
(4) A(エ) B(ウ) C(エ)
※ 理想気体は分子間力が無いため液化しないが空気を読んでジエチルエーテルが液化するとした。
(5) A(イ) B(オ) C(イ)
(6) A(エ) B(エ) C(イ)
(7) A(エ) B(オ) C(ウ)
(8) A(エ) B(ウ) C(イ)
(9) A(エ) B(ア) C(オ)
(10) A(イ) B(エ)※ C(エ)
※ B:フェニルアラニンの呈色は弱いが、それでも硝酸を加えた後塩基性条件にすれば橙色を示す。ベンゼン環を含むアミノ酸(チロシン・フェニルアラニン・トリプトファン)は全てOKとしてよい。
※ C : 環状構造はアミノ基がペプチド結合に使われるためニンヒドリン反応を起こさないが、リシンは側鎖にアミノ基をもつのでニンヒドリン反応を起こす。
第2問
問1 (カ)
問2 (イ)(カ)
問3 ① $m$ ② $\dfrac{n+2m}{2}$ ③ $m$
④ $\ce{H2O}$ ⑤ $\ce{CO2}$
問4 陽極 $\ce{2Cl- -> Cl2 + 2e-}$
陰極 $\ce{2H2O +2e^- -> H2 + 2OH-}$
問5 水素 $\pu{1.5E-1 mol}$
削減率 $5.3$ %
更新前 $4.5$ %としていたのは
$\dfrac{800}{890}\times(1-\dfrac{x}{100})=1-0.149$ の計算を途中3桁ではなく2桁(0.149を0.15など)で計算していたためでした。
申し訳ありません。
問6 $\ce{Fe2O3 + 3CO -> 2Fe + 3CO2}$
$\ce{Fe2O3 + 3H2 -> 2Fe + 3H2O}$
問7 $\pu{1.2E-1 mol}$
問8 (カ)
問9 (オ)
第3問
問1 $\ce{C9H8O4}$
問2 アセチルサリチル酸
問3 (ア)
問4 $\ce{Al(OH)3 + 3HCl -> AlCl3 + 3H2O}$
$\ce{Al(OH)3 + NaOH -> Na[Al(OH)4]}$
問5 $65$ % ※02/17訂正
市販薬を入れずに滴定すると、塩酸が余分に $\pu{1 mL}$ 消費される。
中和の式を立てる際には、この消費分を足す必要がある。
水酸化ナトリウム水溶液と市販薬を入れた溶液を加熱しているのでアセチルサリチル酸が加水分解される。
$\ce{C6H4(OCOCH3)COOH + 2NaOH ->}$
$\ce{C6H4(OH)COONa + CH3COONa}$
市販薬に含まれるアセチルサリチル酸を $x$$\pu{ [g]}$ とおくと、
$\ce{0.5 \times \dfrac{3.2+1.0}{1000} + 2\times\dfrac{x}{180} = 0.50 \times \dfrac{10}{1000}}$
$x=0.261$
$\dfrac{0.261}{0.40}\times100=65.2 \cdots$
よって $65$ (%)
※なお、フェノール性ヒドロキシ基が水酸化ナトリウムで中和されたとしても、加えられた塩酸によって弱酸遊離反応を起こすため、ヒドロキシ基はもとに戻る。ゆえに必要な塩酸の量は変化しない。
問6 $9$ 種類
問7 ベンゼン環を $\ce{Ph}$ で表すと、
$\ce{Ph – CH2 – CH2 -OH}$
$\ce{Ph – CH(OH) -CH3}$
$\ce{Ph – CH2 – O -CH3}$
$\ce{Ph – O – CH2 -CH3}$
問8
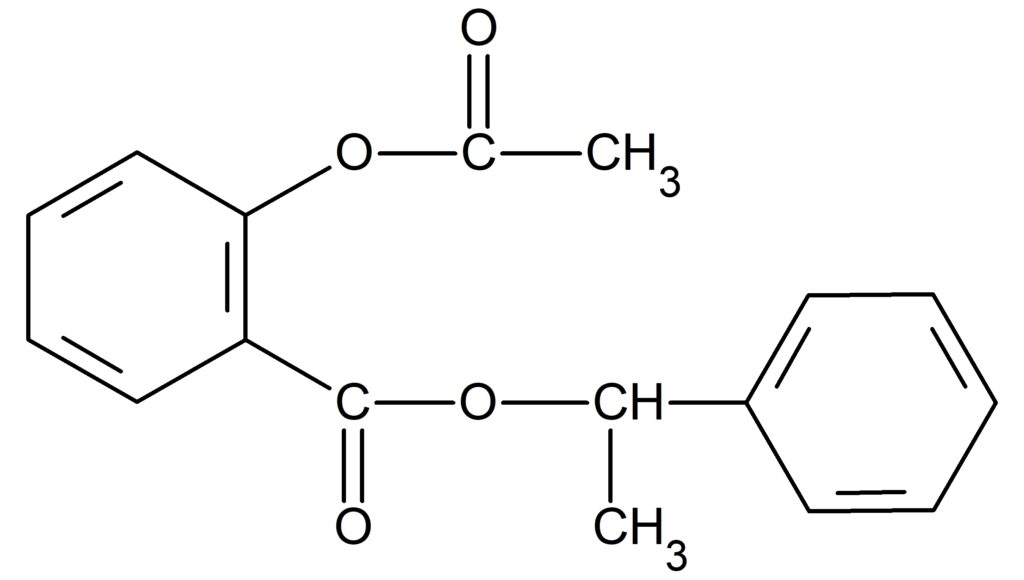
問9
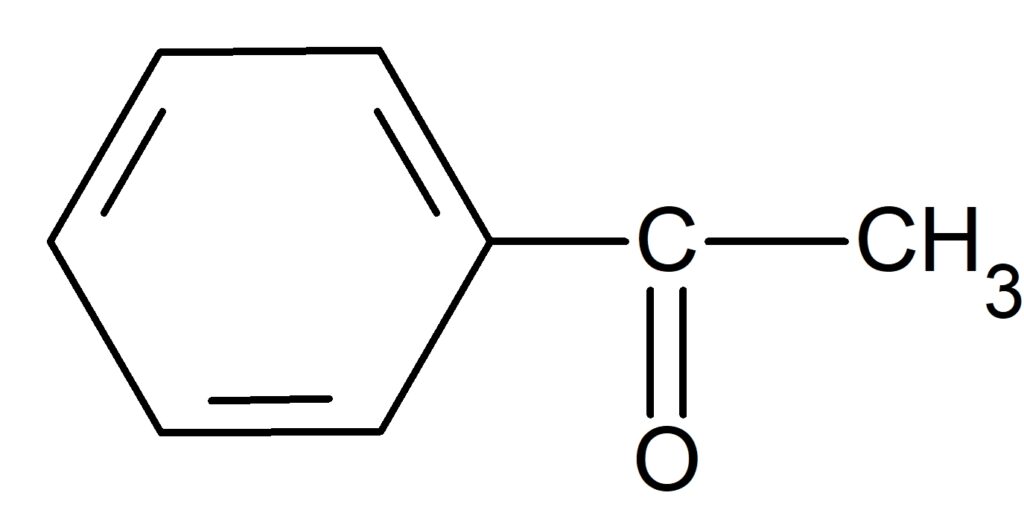
※ 問8、問9
硫酸酸性二クロム酸カリウム水溶液で酸化とあるが、 $\ce{C8H10O}$(芳香族)の 第1級アルコールをカルボン酸まで酸化すると、銀鏡反応は陰性である。
第2級アルコールは酸化するとケトンになるため、銀鏡反応によって区別がつかない。
穏やかに酸化していると考えれば、第1級アルコールはアルデヒドとなるので区別がつく。よって上記の解答とした。



